Ngày 24/05/2019, FDA đã phê duyệt Piqray (alpelisib; Novartis) sử dụng kết hợp với fulvestrant trong điều trị ung thư vú giai đoạn di căn hay tiến xa có thụ thể hormon dương tính (HR+), HER2 (-) và có đột biến PIK3CA sau khi đã tiến triển với phác đồ nội tiết.
Alpelisib là một chất ức chế phosphatidylinositol-3-kinase (PI3K). Trên tế bào ung thư vú, alpelisib ức chế quá trình phosphoryl hóa của các đích cuối trên gen PIK3CA (phosphatidylinositol-4,5-bisphosphate 3-kinase), bao gồm Akt và thể hiện tác dụng trên dòng tế bào ung thư có đột biến PIK3CA.

Bệnh nhân ung thư vú có thụ thể hormon dương tính giai đoạn di căn thường có khối u di căn xa ở xương, phổi, gan và não, được điều trị với liệu pháp hormon có hoặc không có kết hợp với hóa trị. Hiện nay, trên nhóm bệnh nhân ung thư vú giai đoạn di căn hay tiến xa có thụ thể hormon dương tính, đột biến PIK3CA chiếm khoảng 40%. Bệnh nhân có đột biến PIK3CA thường tiến triển khối u nhanh hơn, kháng với điều trị nội tiết và có tiên lượng nghèo nàn.
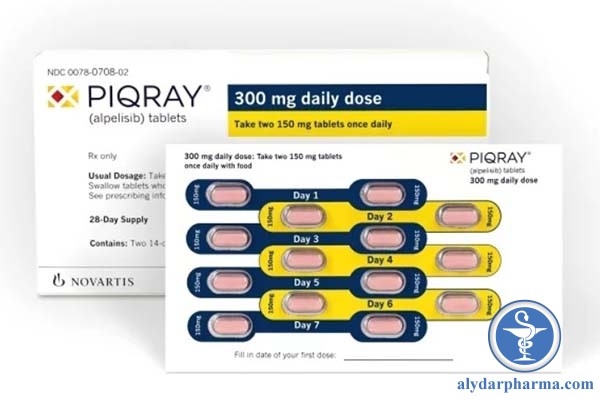
Phê duyệt Alpelisib dựa trên thử nghiệm SOLAR-1 tiến hành trên 527 bệnh nhân ung thư vú giai đoạn tiến xa hay di căn có HR(+), HER (-) đã tiến triển hay tái phát sau khi được điều trị với chất ức chế aromatase. Bệnh nhân trong nghiên cứu được phân ngẫu nhiên vào hai nhóm, nhóm được điều trị với Piqray kết hợp fulvestrant và nhóm điều trị placebo kết hợp fulvestrant. Tiêu chí chính của nghiên cứu là thời gian sống không bệnh tiến triển (PFS – Progress Free Survival) trên nhóm bệnh nhân có đột biến PIK3CA (n=341).
Trên nhóm bệnh nhân đột biến PIK3CA được điều trị với Piqray kết hợp fulvestrant có trung vị PFS là 11 tháng, trong khi nhóm bệnh nhân được điều trị placebo kết hợp fulvestrant có trung vị PFS là 5,7 tháng ([HR] 0,65; 95% CI: 0,50-0,85; P =0,0013); tuy nhiên, PFS không có lợi khi quan sát trên nhóm bệnh nhân không có đột biến PIK3CA (HR=0,85; 95% CI: 0,58-1,25).
Ngoài ra, tỷ lệ đáp ứng chung (ORR – Overall response rate), được định nghĩa là tỷ lệ bệnh nhân có giảm ít nhất 30% kích thước khối u, cao hơn ở nhóm bệnh nhân được điều trị kết hợp Piqray và fulvestrant so với nhóm bệnh nhân sử dụng placebo và fulvestrant, tỷ lệ lần lượt ở hai nhóm là 35,7% và 16,2% (P=0,0002).
TS.Fabrice André – Giám đốc nghiên cứu INSERM Unit U981, Giáo sư tại phòng ung thư lâm sàng của Hiệp hội Gustave Roussy ở Villejuif, Pháp, nhà điều tra chính về thử nghiệm SOLAR-1 đã đánh giá: “Kết quả thử nghiệm pha III SOLAR-1 đã cho thấy, sử dụng kết hợp Piqray và fulvestrant trên bệnh nhân có đột biến PIK3CA làm cải thiện trung vị PFS và cả ORR gấp đôi so với nhóm bệnh nhân chỉ sử dụng fulvestrant, điều này mang đến hy vọng sẽ kéo dài thời gian sống không bệnh tiến triển hơn cho bệnh nhân”;
“ Phê duyệt Piqray dẫn đến thay đổi lớn quan điểm điều trị ung thư vú của các nhà lâm sàng, cần tiến hành xét nghiệm đột biến PIK3CA và có chiến lược điều trị dựa trên hồ sơ bộ gen của bệnh nhân ung thư vú”.
Về tính an toàn của alpelisib, các tác dụng phụ ghi nhận chủ yếu trong thử nghiệm là tăng đường huyết, tăng creatinin, tiêu chảy, ban da, giảm số lượng bạch cầu, tăng GGT, nôn và buồn nôn, chán ăn, tăng ALT, mệt mỏi, tăng lipase, giảm hemoglobin, viêm dạ dày, giảm cân, giảm canxi, kéo dài aPTT, rụng tóc.
Piqray được bào chế dưới dạng viên nén có ba mức liều là 50mg, 150mg và 200 mg.

Thông tin chi tiết thêm về Piqray trên trang https://www.pharma.us.novartis.com/.
DS Nguyễn Thị Uyên tổng hợp và dịch thuật
Nguồn : pi3k-inhibitor-breast-cancer
Namud Insider